Viên nén Bosentan - Thuốc điều trị tăng huyết áp động mạch phổi
Thông tin dành cho chuyên gia
Bosentan là một chất đối kháng thụ thể endothelin kép được sử dụng để điều trị tăng huyết áp động mạch phổi (PAH). |
Nguồn gốc: Bosentan là một chất đối kháng thụ thể endothelin kép được bán trên thị trường dưới tên thương mại Tracleer bởi Actelion Pharmaceuticals. Bosentan đã được nghiên cứu về bệnh suy tim trong một thử nghiệm được gọi là REACH-1 đã kết thúc sớm vào năm 1997, do độc tính ở liều đang được nghiên cứu. Nó đã được chấp thuận cho tăng áp động mạch phổi ở Hoa Kỳ vào tháng 11 năm 2001, và ở Liên minh Châu Âu vào tháng 5 năm 2002.
Nhóm: Thuốc kê đơn - Rx
1. Tên hoạt chất
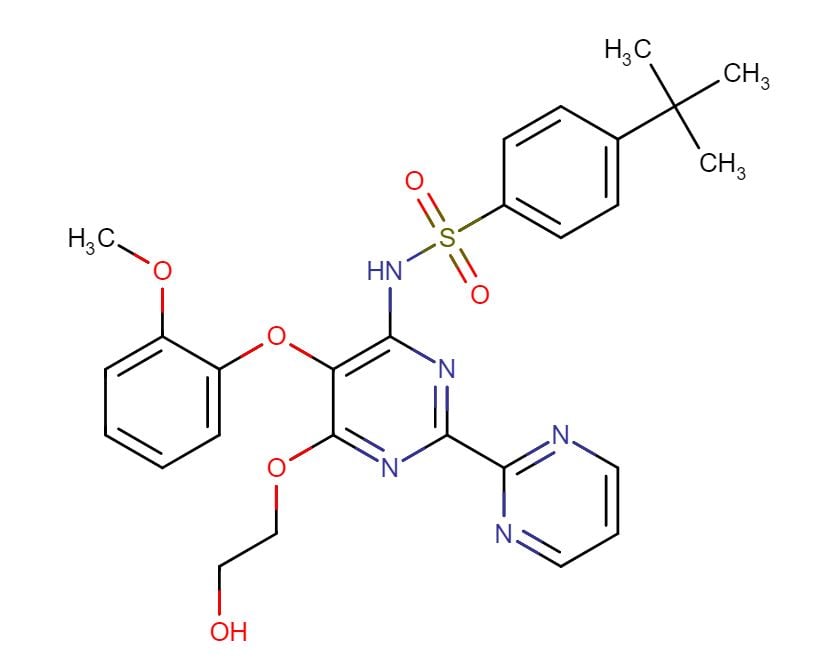
Bosentan
Tên biệt dược thường gặp: Tracleer, Bosentan, Maosenbo 125,Maosenbo 62,5,Misenbo 125,Misenbo 62,5,Safebo 125,Safebo 62,5,Trasenbin 62,5,...

2. Dạng bào chế
Dạng bào chế: Viên nén.
Các loại hàm lượng:
Viên nén 62,5 mg, 125 mg.
3. Chỉ định
Điệu trị tăng huyết áp động mạch phổi (Nhóm I tổ chức y tế thế giới) ở bệnh nhân có các triệu chứng nhóm III hoặc IV Tổ chức y tế thế giới, để cải thiện khả năng luyện tập và làm giảm tỷ lệ trường hợp xấu về lâm sàng.
4. Dược lực và dược động học
4.1. Dược lực
Nhóm dược lý: Thuốc điều trị tăng áp mạch phổi nhóm đối kháng thụ thể Endothelin.
Bosentan được sử dụng để điều trị tăng huyết áp động mạch phổi (PAH, cao huyết áp trong các mạch mang máu đến phổi). Bosentan là thuốc đối kháng thụ thể endothelin. Nó hoạt động bằng cách ngăn chặn các hành động của endothelin, một chất tự nhiên mà làm cho mạch máu bị thu hẹp và ngăn chặn lưu lượng máu ở những người có PAH.
Cơ chế tác dụng:
Endothelin – 1 (ET – 1) là một hormon thần kinh tác dụng bởi sự gắn kết với thụ thể ETA và ETB ở nội bộ và cơ trơn mạch. Nồng độ ET – 1 tăng lên trong huyết tương và mô phổi của bệnh nhân tăng huyết áp động mạch phổi, gợi ý về vai trò gây bệnh của ET-1. Bosentan là một thuốc đối kháng đặc hiệu và cạnh tranh ở các thụ thể của endothelin tuýp ETA và ETB. Bosentan có ái lực hơi cao hơn đối với thụ thể ETA so với thụ thể ETB.
4.2. Dược động học
Hấp thu
Sinh khả dụng tuyệt đối của Bosentan ở người tình nguyện bình thường khoảng 50% và không bị ảnh hưởng bởi thức ăn. Nồng độ đỉnh trong huyết tương đối đạt đươc trong khoảng 3-5 giờ sau khi uống 1 liều.
Ở người khỏe mạnh, sau khi uống, nồng độ trong huyết tương đối đa của Bosentan đạt được trong vòng 3 – 5 giờ và thời gian bán thải khoảng 5 giờ. Ít dữ liệu trên bệnh nhân cho thấy sự lưu lại trong Bosentan trong cơ thể bệnh nhân tăng huyết áp động mạch phổi lớn hơn khoảng 2 lần so với người lớn khỏe mạnh.
Phân bố
Thể tích phân bố khoảng 18 lít. Bosentan gắn kết ở mức cao (>98%) với protein huyết tương, chủ yếu với albumin. Bosentan không thâm nhập vào hồng cầu.
Chuyển hóa
Bosentan được chuyển hóa ở gan. bosentan có 3 chất chuyển hóa, một chất có hoạt tính dược lý và có thể đóng góp 10-20% vào tác dụng của Bosentan. Bosentan là chất gây cảm ứng enzym CYP2C9 và CYP3A4 và có thể cả CYP2C19.
Thải trừ
Sự thanh thải toàn phần sau khi 1 liều tiêm tĩnh mạch khoảng 4 lit/giờ ở bệnh nhân có tăng huyết áp động mạch phổi. khi uống thuốc nhiều liều, nồng độ trong huyết tương ở người lớn khỏe mạnh giảm dần đến 50 -65 % nồng độ nhận thấy sau khi dùng liều đơn, có thể do tác dụng tự cảm ứng của enzym chuyển hóa ở gan. trạng thái ổn định đạt được trong vòng 3 – 5 ngày. Bosentan được thải trừ do sự bài tiết trong mật sau khi được chuyển hóa ở gan. Dưới 3% của một liều uống được bài tiết trong nước tiểu. Thời gian bán thải khoảng 5 giờ.
* Đối tượng đặc biệt
Bệnh nhân suy thận
Trên bệnh nhân suy thận nặng (độ thanh thải creatinin 15-30mL/phút), nồng độ bosentan thấp hơn khoảng 10%. Nồng độ chất chuyển hóa bosentan trong huyết tương khoảng gấp đôi so với người tình nguyện khỏe mạnh có chức năng thận bình thường.
Không có kinh nghiệm đặc biệt trên bệnh nhân lọc máu. Do đặc tính hóa lý và tỉ lệ liên kết cao với protein huyết tương, có thể suy ra rằng tỉ lệ lớn bosentan không thể bị lọc khỏi tuần hoàn hệ thống bằng lọc máu (xem phần “Chế độ liều và cách sử dụng”).
Bệnh nhân suy gan: Không có thay đổi dược động học đáng kể trên bệnh nhân suy gan nhẹ (Child-Pugh độ A). Trên những bệnh nhân này, diện tích dưới đường cong ở trạng thái cân bằng bằng 9% so với bosentan và 33% so với chất chuyển hóa chính Ro 48-5033, so với người tình nguyện khỏe mạnh. Dược động học của bosentan không được nghiên cứu trên bệnh nhân suy gan phân loại Child-Pugh B hoặc C.
Trẻ em và trẻ vị thành niên
Dược động học sau khi dùng đường uống đơn liều hoặc đa liều được nghiên cứu trên bệnh nhi tăng áp lực động mạch phổi trẻ em hoặc trẻ vị thành niên, liều được tính theo cân nặng cơ thể (BREATHE-3 xem phần “Dược động học”). Sinh khả dụng hệ thống của bosentan giảm theo thời gian, do tương ứng với việc kích ứng các enzym đã biết của bosentan.
5. Lâm sàng
5.1. Liều dùng
Liều dùng này áp dụng với dạng viên nén 62,5 mg, 125 mg. Phải uống viên vào buổi sáng và buổi chiều, cùng hoặc không cùng với thức ăn.
Bệnh nhân trên 12 tuổi:
- Bắt đầu điều trị với Bosentan 62,5 mg x 2 lần/ngày.
- Người có thể trọng thấp (<40 kg), liều khởi đầu và liều duy trì là 62.5 mg x 2 lần/ ngày.
Trẻ em: Liều khuyến cáo cho trẻ em 1 tháng tuổi – 12 tuổi.
- 10 – 20 kg: khởi đầu 31,25 mg/lần/ngày, sau 4 tuần tăng đến liều duy trì 31,25 mg x 2 lần/ngày.
- 20 – 40 kg: khởi đầu 31,25 mg x 2 lần/ngày, sau 4 tuần tăng đến liều duy trì 62,5 mg x 2 lần/ngày.
- Trên 40 kg: khởi đầu 62,5mg x 2 lần/ngày. sau 4 tuần tăng đến liều duy trì 125 mg x 2 lần/ ngày.
Bệnh nhân suy thận: không cần điều chỉnh liều.
5.2. Chống chỉ định
- Mẫn cảm với Bosentan hay bất kỳ thành phần nào của thuốc
- Phụ nữ có thai
- Dùng đồng thời với Cyclosporin A ( gây tăng rõ rệt nồng độ huyết tương của Bosentan), glyburic ( tăng nguy cơ tăng các enzym gan).
- Suy gan vừa hoặc nặng, bệnh nhân có aminotransferase cao (> 3 x ULN).
5.3. Thận trọng
Thận trọng khi sử dụng trong trường hợp:
- Không được bắt đầu điều trị với Bosentan nếu huyết áp tâm thu dưới 85 mmHg.
- Bosentan chống chỉ định với những bệnh nhân suy gan vừa và nặng. Nồng độ aminotransferase gan nên được đo trước khi bắt đầu điều trị, 1 lần/ tháng trong quá trình điều trị và 2 tuần sau khi tăng liều.
- Không nên bắt đầu điều trị với Bosentan ở những bệnh nhân có nồng độ aminotransferase cao gấp 3 lần giới hạn trên.
- Nếu nồng độ aminotransferase cao gấp 3-5 lần trong quá trình điều trị, nên ngưng sử dụng Bosentan hay giảm liều và theo dõi nồng độ aminotransferase mỗi 2 tuần. Nếu mức aminotransferase trở về trị số trước điều trị, có thể tiếp tục liệu pháp điều trị hay bắt đầu lại, nhưng nồng độ aminotransferase nên được kiểm tra sau 3 ngày, sau 2 tuần và mỗi tháng.
- Nếu nồng độ aminotransferase tăng gấp 5 – 8 lần, nên ngưng dùng Bosentan và theo dõi nồng độ aminotransferase mỗi 2 tuần. khi các mức aminotransferase trở về trị số trước điều trị, xem xét việc điều trị trở lại.
- Nếu nồng độ tăng hơn 8 lần hay có những triệu chứng của độc gan hay tăng bilirubin toàn phần cao gấp 2 lần, ngưng điều trị và không xem xét việc điều trị trở lại Bosentan.
- Cần theo dõi nồng độ Hemoglobin sau 1 và 3 tháng điều trị sau đó cứ 3 tháng một lần trong suốt quá trình điều trị. Nếu giảm rõ rệt nồng độ hemoglobin, cần đánh giá thêm để xác định nguyên nhân và nhu cầu về trị liệu đặc hiệu.
- Không nên dùng Bosentan ở những bệnh nhân hạ huyết áp. Mặc dù không có bằng chứng về sự hồi ứng cấp tính sau khi ngưng Bosentan, để tránh khả năng xấu đi về lâm sàng, nên giảm liều từ từ.
- Nếu các dấu hiệu của phù phổi xảy ra khi dùng Bosentan, cần xem xét khả năng có bệnh tắc tĩnh mạch phổi kết hợp và phải ngưng dùng bosentan.
- Thận trọng lựa chọn liều đối với bệnh nhân cao tuổi, xét đến tần số cao giảm chức năng gan, thận hoặc tim, các bệnh mắc đồng thời hoặc điều trị với các thuốc khác.
- Bosentan và những thuốc đối kháng thụ thể Endothelin gây quái thai ở chuột và không nên dùng cho phụ nữ mang thai hay phụ nữ có khả năng sinh đẻ nhưng không sử dụng phương pháp tranh thai tin cậy. Các biện pháp tránh thai nội tiết có thể không đầy đủ.
Tác động của thuốc trên người lái xe và vận hành máy móc.
Cần thận trọng khi sử dụng cho các đối tượng lái xe và vận hành máy móc.
5.4. Tác dụng không mong muốn
Tác dụng phụ được báo cáo bao gồm nhức đầu, viêm mũi – họng, đỏ bừng mặt, phù nề, hạ huyết áp, chóng mặt, đành trống ngực, rối loạn tiêu hóa, ngưa, phát ban, mệt mỏi, chuột rút, thiếu máu.
Sốc phản vệ và phù mạch hiếm khi được báo cáo.
Tăng Enzym gan phụ thuộc liều có thể xảy ra, bất thường chức năng gan, xơ gan và suy gan đã được báo cáo.
Bosentan gây thái quai ở động vật.
Việc đánh giá các phản ứng có hại dựa trên định nghĩa tần suất sau:
- (1) Rất phổ biến: ≥1/10;
- (2) Phổ biến: ≥1/100 đến <1/10;
- (3) Không phổ biến: ≥1/1.000 đến <1/100;
- (4) Hiếm: ≥1/10.000 đến <1/1.000;
- (5) Rất hiếm: <1/10.000;
- (6) Không rõ: không thể ước tính từ dữ liệu có sẵn
| Hệ cơ quan | TDKMM | (1) | (2) | (3) | (4) | (5) | (6) |
| Hệ miễn dịch | Phản ứng quá mẫn (bao gồm viêm da, ngứa và phát ban) | x | |||||
| Sốc phản vệ | x | ||||||
| Hệ thần kinh | Nhức đầu, ngất | x | |||||
| Mắt | Nhìn mờ | x | |||||
| Tim | Đánh trống ngực | x | |||||
| Mạch máu | Đỏ bừng mặt, hạ huyết áp | x | |||||
| Phù, giữ nước | x | ||||||
| Hệ máu và hạch bạch huyết | Thiếu máu, giảm hemoglobin | x | |||||
| Giảm tiểu cầu. Giảm bạch cầu trung tính, giảm bạch cầu | x | ||||||
| Thiếu máu hoặc hemoglobin giảm cần truyền hồng cầu | x | ||||||
| Hệ hô hấp, lồng ngực và trung thất | Nghẹt mũi | x | |||||
| Hệ tiêu hóa | Bệnh trào ngược dạ dày thực quản. Tiêu chảy | x | |||||
| Da và mô dưới da | Phát ban | x | |||||
| Cơ, xương | Đau khớp, rối loạn cơ | ||||||
| Gan, mật | Kiểm tra chức năng gan bất thường | x | |||||
| Tăng aminotransferase liên quan đến viêm gan (bao gồm cả đợt cấp có thể có của bệnh viêm gan tiềm ẩn) và/hoặc vàng da | x | ||||||
| Xơ gan, suy gan | x | ||||||
| Khác |
Thông báo cho Bác sĩ những tác dụng không mong muốn gặp phải khi sử dụng thuốc.
5.5. Khả năng sinh sản, mang thai và cho con bú
Thai kỳ
Bosentan có thể gây độc hại cho thai, vì vậy chống chỉ định đối với thai ky. phải loại trừ thai nghén trước khi bắt đầu điều trị với Bosentan, sau đó dự phòng bằng biện pháp tránh thai chắc chắn. chỉ bắt đầu điều trị Bosentan ở phụ nữ có khả năng mang thai sau một xét nghiệm thai nghén âm tính và chỉ ở phụ nữ áp dụng phương pháp tránh thai đầy đủ ngoài thuốc tránh thai nội tiết tố.
Cho con bú
Thời kỳ cho con bú: không biết thuốc có bài tiết trong sữa hay không. vì nhiều thuốc được bài tiết trong sữa người, không nên cho con bú trong thời gian dùng thuốc.
Khả năng sinh sản
Các nghiên cứu trên động vật cho thấy tác dụng đối với tinh hoàn. Trong một nghiên cứu điều tra tác động của bosentan đối với chức năng tinh hoàn ở bệnh nhân PAH nam, 8 trong số 24 bệnh nhân cho thấy nồng độ tinh trùng giảm so với ban đầu ít nhất là 42% sau 3 hoặc 6 tháng điều trị với bosentan. Dựa trên những phát hiện này và dữ liệu tiền lâm sàng, không thể loại trừ rằng bosentan có thể có tác động bất lợi đến quá trình sinh tinh ở nam giới. Ở trẻ em nam, không thể loại trừ ảnh hưởng lâu dài đến khả năng sinh sản sau khi điều trị bằng bosentan.
5.6. Tương tác thuốc
- Cytochrom P450: Bosentan được chuyển hóa bởi CYP2C9 và CYP3A. Dùng đồng thời chất ức chế CYP2C9 ((fluconazol hoặc amiodaron) và chât ức chế manh CYP3A (ketoconazol, itraconazol) hoặc chất ức chế trung bình CYP3A (amprenavir, erythromycin, fluconazol, diltiazem) với Bosentan có thể làm gia tăng nồng độ Bosentan trong huyết tương. Không khuyến cáo phối hợp cùng một chát ức chề CYP2C9 và một chất ức chế CYP3A mạnh hoặc trung bình với Bosentan.
- Bosentan là một chất cảm ứng CYP3A và CYP2C9. Do đó nồng độ trong huyết tương của thuốc được chuyển hóa bởi hai isozym này sẽ giảm khi dùng cùng với Bosentan. Bosentan không có tác dụng ức chế bất kỳ Isozym CYP invitro (CYP1A2, CYP2C1, CYP2C19, CYP2D6, CYP3A). Do đó, Bosentan không làm tăng nồng độ trong huyết tương của các thuốc chuyển hóa bởi các enzym này.
- Cyclosporin A: nồng độ Bosentan trong huyết tương tăng trong khi nồng độ Cyclosporin giảm, vì vậy chống chỉ định khi dùng đồng thời Bosentan và Cyclosporin A.
- Tacrolimus: dùng đồng thời Bosentan và tacrolimus trên động vật làm tăng rõ rệt nồng độ huyết tương của Bosentan. Cần phải thận trọng nếu dùng đồng thời.
- Glyburid: tăng nguy cơ tăng aminotransferase gan ở bệnh nhân dùng đồng thời bosentan với Glyburid. Chống chỉ định dùng kết hợp và xem xét dùng các thuốc hạ đường huyết khác. việc dùng đồng thời làm giảm nồng độ huyết tương của Bosentan, glyburid cũng như các thuốc hạ đường huyết uống khác được chuyển hóa chủ yếu bởi CYP2C9 hoặc CYP3A4. Caafn phải xem xét khả năng sự kiểm soát đường huyết ở bệnh nhân dùng các thuốc này.
- Kotoconazol: làm tăng nồng độ huyết tương của Bosentan. Không cần phải điều điều chỉnh liều Bosentan nhưng phải xem xét khả năng tăng tác dụng của Bosentan.
- Simvastin và các statin khác: dùng đồng thời làm giảm nồng độ huyết tương của simvastatin và các statin khác được chuyển hóa CYP3A4. Cần xem xét khả năng giảm hiệu lực của statin, theo dõi nồng độ Cholesterol huyết sau khi bắt đầu dùng Bosentan và điều chỉnh liều statin nếu cần thiết.
- Warfarin: dùng đồng thời làm giảm nồng độ huyết tương của warfarin. Kinh nghiệm lâm sàng không cho thấy thay đổi có liên quan về lâm sàng ở INR hoặc liều warfarin. vì warfarin có chỉ số điều trị hẹp, cần theo dõi những thông số đông máu và chỉnh liều warfarin nếu cần.
- Digoxin, nimodipin và losartan: Bosentan không có tương tác dược động học có ý nghĩa digoxin và nimodipin; losartan không có tác dụng có ý nghĩa trên nồng độ huyết tương của Bosentan.
- Sildenafil: dùng đồng thời làm giảm nồng độ huyết tương của sidenafil và tăng nồng độ huyết tương của Bosentan. Cẩn thận trọng khi dùng kết hợp, theo dõi những phản ứng lâm sàng và tác dụng phụ, chỉnh liều nếu cần thiết.
- Rifampicin: dùng đồng thời làm tăng nồng độ đấy của Bosentan sau liều dùng đồng thời đầu tiên nhưng làm giảm nồng độ Bosentan ở trạng thái ổn định. Theo dõi chức năng gan hàng tuần trong 4 tuần đầu tiên, sau đó hàng tháng.
- Các thuốc tránh thai hormon: một nghiên cứu về tương tác đã chứng minh rằng việc dùng đồng thời Bosentan với thuốc tránh thai hormon uống gây giảm trung bình nồng độ Norethindron và ethinyl estradiol tương ứng 14% và 31%. Tuy nhiên, mức giảm phơi nhiễm tương ứng là 56% và 66%. vì vậy, các thuốc tránh thai hormon bao gồm các dạng thuốc uống, tiêm, chân bì và cấy dưới da có thể không chắc chắn khi dùng chung với bosentan.
- Lopinavir/ Ritonavir hay phát đồ điều trị HIV có Ritonavir khác: dữ liều Invitro cho thấy Bosentan là chất nền của protein vận chuyển anion hữu cơ (Organic Anion Transport Protein – OATP), CYP3A, CYP2C9. Ritonavir ức chế OATP và CYP3A. Tuy nhiên, tác động của ritonavir trên dược động học bosentan phần lớn do ảnh hưởng của nó trên OATP. trên những tình nguyện viên bình thường, dùng đồng thời Bosentan 125mg/2 lần/ngày với lopinavir 400 mg/ ritonavir 100 mg x 2 lần/ngày làm tăng nồng độ đáy của bosentan vào ngày thứ 4 và thứ 10 tương ứng khoảng 48 lần và 5 lần so với những người chỉ dùng Bosentan. Vì vậy, cần điều chỉnh liều Bosentan khi bắt đầu dùng Lopinavir/ritonavir. Chỉ định đồng thời Bosentan 125 mg/2 lần/ngày không có tác động đáng kể trên dược động học của lopinavir 400 mg/ritonavir 100 mg x 2 lần/ ngày.
5.7. Quá liều
Các triệu chứng
Tác dụng không mong muốn thường gặp nhất là nhức đầu nhẹ đến vừa, nôn, buôn nôn, chóng mặt, mờ mắt, tăng nhịp tim. Quá liều lớn có thể dẫn đến hạ huyết áp rõ rệt cần sự hỗ trợ tim mạch tích cực.
Xử trí
Không có kinh nghiệm riêng biệt về quá liều Bosentan. Điều trị triệu chứng.
Bệnh nhân hồi phục hoàn toàn trong vòng 24 giờ sau khi được hỗ trợ huyết áp. Không thể sử dụng các biện pháp lọc máu với bệnh nhân quá liều bosentan.



Viết bình luận